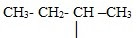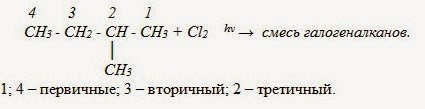10 класс. Химия. Алканы
10 класс. Химия. Алканы
Комментарии преподавателя

В таблице представлены некоторые представители ряда алканов и их радикалы.
|
Формула |
Название |
Название радикала |
|
CH4 |
метан |
- CH3 метил |
|
C2H6 |
этан |
- C2H5 этил |
|
C3H8 |
пропан |
- C3H7 пропил |
|
C4H10 |
бутан |
- C4H9 бутил |
|
C4H10 |
изобутан |
изобутил |
|
C5H12 |
пентан |
пентил |
|
C5H12 |
изопентан |
изопентил |
|
C5H12 |
неопентан |
неопентил |
|
C6H14 |
гексан |
гексил |
|
C7H16 |
гептан |
гептил |
|
C10H22 |
декан |
децил |
Тренажёр "Гомологический ряд алканов"
Из таблицы видно, что эти углеводороды отличаются друг от друга количеством групп - СН2 -.Такой ряд сходных по строению, обладающих близкими химическими свойствами и отличающихся друг от друга числом данных групп называется гомологическим рядом. А вещества, составляющие его называются гомологами.
Гомологи – вещества сходные по строению и свойствам, но отличающиеся по составу на одну или несколько гомологических разностей (- СН2 -)

Углеродная цепь - зигзаг (если n ≥ 3)
σ – связи (свободное вращение вокруг связей)
длина (-С-С-) 0,154 нм
энергия связи (-С-С-) 348 кДж/моль
Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации
угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг). Длина связи С-С в предельных углеводородах равна 0,154 нм (1нм=1*10-9м).
а) электронная и структурная формулы;
б) пространственное строение

Тренажёр "Состав и строение алканов"
4. Изомерия – характерна СТРУКТУРНАЯ изомерия цепи с С4
Один из этих изомеров (н-бутан) содержит неразветвленную углеродную цепь, а другой — изобутан — разветвленную (изостроение).
Атомы углерода в разветвленной цепи различаются типом соединения с другими углеродными атомами. Так, атом углерода, связанный только с одном другим углеродным атомом, называется первичным, с двумя другими атомами углерода – вторичным, с тремя – третичным, с четырьмя – четвертичным.
С увеличением числа атомов углерода в составе молекул увеличиваются возможности для разветвления цепи, т.е. количество изомеров растет с ростом числа углеродных атомов.
Сравнительная характеристика гомологов и изомеров
1. Свою номенклатуру имеют радикалы (углеводородные радикалы)
2. Число одинаковых заместителей указывают при помощи множительных приставок:
два – «ди»
три – «три»
четыре – «тетра»
пять – «пента»
шесть – «гекса»
семь – «гепта»
восемь – «окта»
девять – «нано»
Для названия предельных углеводородов применяют в основном систематическую(международная номенклатура IUPAC) и рациональную номенклатуры.
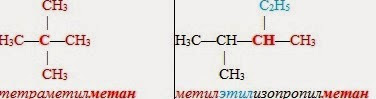
I. По рациональной номенклатуре алканы рассматривают как производные простейшего углеводорода — метана, в молекуле которого один или несколько водородных атомов замещены на радикалы. Эти заместители (радикалы) называют по старшинству (от менее сложных к более сложным). Если эти заместители одинаковые, то указывают их количество. В основу названия включают слово "метан":
II. Систематическая номенклатура
Правила систематической номенклатуры:
1. В формуле молекулы алкана выбираем главную цепь — самую длинную.

2. Затем эту цепь нумеруем с того конца, к которому ближе расположен заместитель (радикал). (Если заместителей несколько, то поступают так, чтобы цифры, указывающие их положение, были наименьшими) Заместители перечисляем по алфавиту.
3. Называем углеводород: вначале указываем (цифрой) место расположения заместителя, затем называем этот заместитель (радикал), а в конце добавляем название главной (самой длинной) цепи.
Таким образом, углеводород может быть назван: 2 - метил - 4 - этилгептан (но не 6-метил-4-этилгептан).
ЦОР:
Образование названий алканов по номенклатуре ИЮПАК
Первичные, вторичные и третичные атомы углерода
Примеры разной записи формул одного и того же вещества
Составление формул алканов по названию
Физические свойства
В обычных условиях
С1- С4 – газы
С5- С15 – жидкие
С16 – твёрдые
Температуры плавления и кипения алканов, их плотности увеличиваются в гомологическом ряду с ростом молекулярной массы. Все алканы легче воды, в ней не растворимы, однако растворимы в неполярных растворителях (например, в бензоле) и сами являются хорошими растворителями. Физические свойства некоторых алканов представлены в таблице.
Таблица 2. Физические свойства некоторых алканов

а) Галогенирование
при действии света - hν или нагревании (стадийно – замещение атомов водорода на галоген носит последовательный цепной характер. Большой вклад в разработку цепных реакций внёс физик, академик, лауреат Нобелевской премии Н. Н. Семёнов )
В реакции образуются вещества галогеналканы RГ или Сn H2n+1Г
(Г - это галогены F, Cl, Br, I)
CH4 + Cl2 hν → CH3Cl + HCl (1 стадия) ;
метан хлорметан CH3Cl + Cl2 hν → CH2Cl2 + HCl (2 стадия);
дихлорметан
СH2Cl2 + Cl2 hν → CHCl3 + HCl (3 стадия);
трихлорметан
CHCl3 + Cl2 hν → CCl4 + HCl (4 стадия).
тетрахлорметан
Скорость реакции замещения водорода на атом галогена у галогеналканов выше, чем у соответствующего алкана, это связано с взаимным влиянием атомов в молекуле:
Электронная плотность связи С – Cl смещена к более электроотрицательному хлору, в результате на нём скапливается частичный отрицательный заряд, а на атоме углерода – частичный положительный заряд.
На атом углерода в метильной группе ( - СН3) создаётся дефицит электронной плотности, поэтому он компенсирует свой заряд за счёт соседних атомов водорода, в результате связь С – Н становится менее прочной и атомы водорода легче замещаются на атомы хлора. При увеличении углеводородного радикала наиболее подвижными остаются атомы водорода у атома углерода ближайщего к заместителю:
CH3 – CH2 – Cl + Cl2 hν → CH3 – CHCl2 + HCl
хлорэтан 1,1 -дихлорэтан
Со фтором реакция идёт со взрывом.
С хлором и бромом требуется инициатор.
Иодирование происходит обратимо, поэтому требуется окислитель для удаления HI из рекции.
Внимание!
В реакциях замещения алканов легче всего замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. Для хлорирования эта закономерность не соблюдается при T>400˚C.
б) Нитрование
(реакция М.И. Коновалова, он провёл её впервые в 1888 г)
CH4 + HNO3(раствор) t˚С → CH3NO2 + H2O
нитрометан
RNO2 или Сn H2n+1 NO2 (нитроалкан)
2. Реакции отщепления (дегидрирование)
а) CnH2n+2 t˚С, Ni или Pd → CnH2n + H2
б) При нагревании до 1500 С происходит образование ацетилена и водорода:
2CH4 1500°С → C2H2 + 3H2
3. Реакции перегруппировки (изомеризация)
н-алкан AlCl3, t°С → изоалкан
4. Реакции горения (горят светлым не коптящим пламенем)
CnH2n+2 + O2 t°С → nCO2 + (n+1)H2O
Помните! Смесь метана с воздухом и кислородом взрывоопасна
V(CH4) : V(O2) = 1: 2
V(CH4) : V(воздуха) = 1 : 10
5. Реакции разложения
а) Крекинг при температуре 700-1000°С разрываются (-С-С-) связи:
C10H22 t°С → C5H12 + C5H10
алкан алкен
б) Пиролиз при температуре 1000°С разрываются все связи,
продукты – С и Н2:
СH4 1000°С → C + 2H2
в) Конверсия метана с образованием синтез – газа (СО + Н2)
CH4 + H2O 800˚C, Ni → СО + 3Н2
Сжиженная пропан-бутановая смесь, горение
Термическое разложение алканов (крекинг)
Тренажёры:
Алканы: строение, номенклатура, получение и физические свойства
Алканы: строение, номенклатура, получение и физические свойства (расчетные задачи)
Определение качественного состава парафина по продуктам окисления
Видео:
Горение парафина в условиях избытка и недостатка кислорода
Горение метана и изучение его физических свойств
Горение твердых углеводородов (на примере парафина)
Установление качественного состава предельных углеводородов
Определение содержания хлора в органических соединениях
Отношение метана к раствору перманганата калия и бромной воде
источники
http://www.youtube.com/watch?t=2&v=P6n4e8aAhs8
http://www.youtube.com/watch?v=SiIEVJHMyxk
http://www.youtube.com/watch?t=8&v=rzdITkWA-hA
http://www.youtube.com/watch?t=8&v=krEf2CEBoRY
источник презентации - http://prezentacii.com/po_himii/2130-alkany.html
http://files.school-collection.edu.ru/dlrstore/0abb145a-4185-11db-b0de-0800200c9a66/x10_029.swf - тренажер
https://sites.google.com/site/himulacom/zvonok-na-urok/10-klass---tretij-god-obucenia- конспект
http://files.school-collection.edu.ru/dlrstore/2416d6cb-aae9-11db-abbd-0800200c9a66/x10_031.swf
http://files.school-collection.edu.ru/dlrstore/0abb6273-4185-11db-b0de-0800200c9a66/x10_041.swf
http://www.youtube.com/watch?t=9&v=oFFqE0OVSMI - заставка